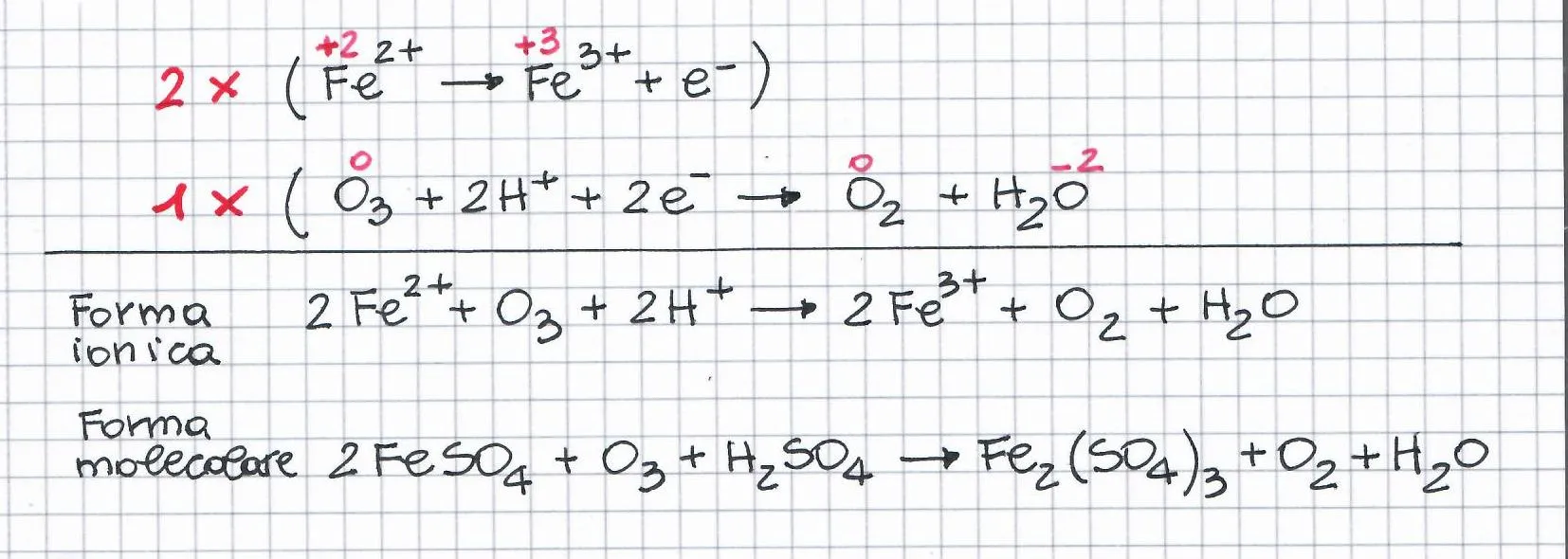1. Bilanciare la seguente reazione (metodo ionico-elettronico): Calcolare il volume di HCl, al 37.0% in peso (d = 1.19 g/mL), r

Bilanciamenti REDOX – Come si risolve un bilanciamento REDOX – metodo delle semireazioni (ionico-elettronico) e metodo del numero di ossidazione – Teoria + esercizi svolti - Il Prof Che Ci Piace